
Проверено фармацевтом
Николаева Елена Юрьевна
В команде с марта 2023 годаФармацевт. Стаж – 43 года
Избранные аптеки
0Москва и Московская область
Москва и Московская область
Клиентский сервис работает с 8.00 до 22.00
Клиентский сервис работает с 8.00 до 22.00
Есть противопоказания, проконсультируйтесь с врачом
Часто ищут в инструкции
Есть противопоказания, проконсультируйтесь с врачом
Цена: 30 502 ₽
Цена действительна при заказе на сайте
Товар добавлен
В корзинуДанный товар есть с меньшим сроком годности
Забронировать по сниженной цене можно по телефону
8 (495) 419 19 19Антибиотик, цефалоспорин.
Зинфоро® вводится внутривенно в виде инфузии в течение 5-60 или 120 минут (см. "Приготовление раствора для инфузий").
Продолжительность терапии должна устанавливаться в зависимости от типа и тяжести инфекции, ответа пациента на терапию.
Режим дозирования у взрослых и пациентов детского возраста
Рекомендованная дозировка препарата Зинфоро® составляет 600 мг каждые 12 часов в виде внутривенной инфузии продолжительностью 5-60 минут (стандартная доза), с соответствующим снижением дозы для пациентов детского возраста (Таблица 2).
Для лечения осложненных инфекций кожи и мягких тканей, доказано или предположительно вызванных Staphylococcus aureus (S. aureus) c MПK цефтаролина < 2 мг/л, дозировка препарата Зинфоро® составляет 600 мг каждые 12 часов в виде внутривенной инфузии продолжительностью 5-60 минут (стандартная доза), с соответствующим снижением дозы для пациентов детского возраста (Таблица 2).
Для лечения пациентов с осложненными инфекциями кожи и мягких тканей, доказано или предположительно вызванными S. aureus с MПK цефтаролина от 2 мг/л до 4 мг/л, дозировка препарата Зинфоро® составляет 600 мг каждые 8 часов в виде внутривенной инфузии продолжительностью 120 минут (высокая доза), с соответствующим снижением дозы для пациентов детского возраста.
Рекомендуемая длительность лечения составляет 5-14 дней для осложненных инфекций кожи и мягких тканей и 5-7 дней для внебольничной пневмонии.
Таблица 2. Дозировка у взрослых с нормальной функцией почек, клиренс креатинина (КК) > 50 мл/мин*
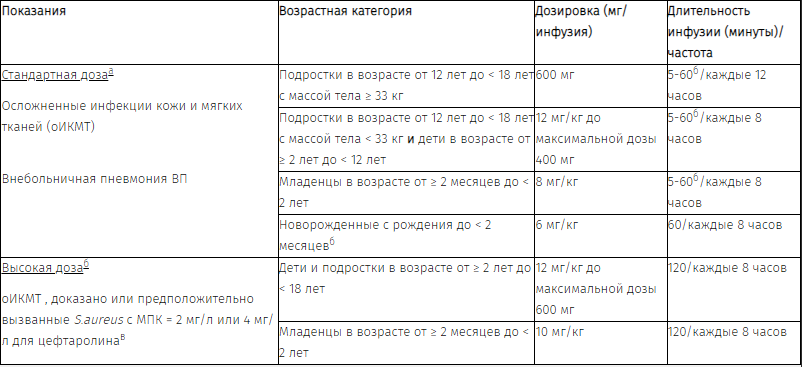
а Для пациентов с клиренсом креатинина, превышающим нормальные значения, получающих стандартную дозу препарата, может быть предпочтительнее длительность инфузии 60 минут.
б Рекомендации по длительности инфузии менее 60 минут и применению высоких доз основаны только на результатах фармакокинетических и фармакодинамических анализов. См разделы Особые указания, Фармакологические свойства.
в Для лечения инфекций, вызванных S.aureus, для которого МПК цефтаролина составляет ≤1 мг/л, рекомендуется стандартная доза препарата.
* Рассчитано по формуле Шварца (в мл/мин/1,73 м2) для пациентов детского возраста.
Применение у особых групп пациентов
Нарушение функции почек
Если КК ≤ 50 мл/мин, дозу препарата следует корректировать в соответствии с информацией, приведенной в Таблицах 4 и 5 (см. раздел «Фармакокинетика»).
Рекомендуемая длительность лечения составляет 5-14 дней для осложненных инфекций кожи и мягких тканей и 5-7 дней для внебольничной пневмонии.
Таблица 4. Дозировка у взрослых с нарушением функции почек, клиренс креатинина (КК) ≤ 50 мл/мин
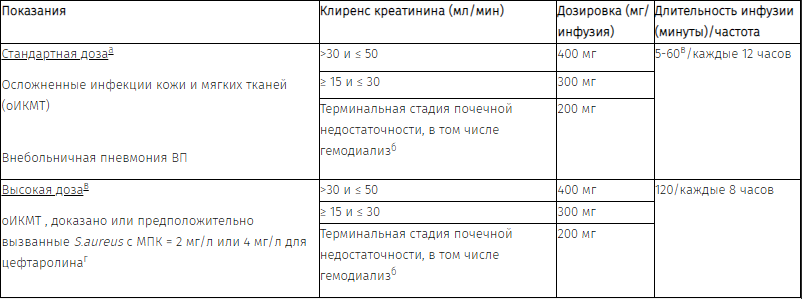
а Рассчитано по формуле Кокрофта - Голта для взрослых. Доза основана на КК. КК следует тщательно контролировать, а дозу препарата следует корректировать в соответствии с функцией почек.
б Цефтаролин выводится при гемодиализе, поэтому препарат Зинфоро® необходимо вводить после выполнения гемодиализа в дни гемодиализа.
в Рекомендации по длительности инфузии менее 60 минут и применению высоких доз основаны только на результатах фармакокинетических и фармакодинамических анализов. См. разделы Особые указания, Фармакологические свойства
г Для лечения инфекций, вызванных S aureus, для которого МПК цефтаролина составляет ≤ 1 мг/л, рекомендуется стандартная доза препарата.
Рекомендации по дозированию у детей и подростков основаны на данных фармакокинетического моделирования. Недостаточно данных, позволяющих рекомендовать коррекцию дозы при терминальной стадии почечной недостаточности у подростков в возрасте от 12 до 18 лет с массой тела менее 33 кг и детей в возрасте от 2 до 12 лет. Недостаточно данных, позволяющих рекомендовать коррекцию дозы у детей в возрасте до 2 лет с нарушением функции почек средней и тяжелой степени, а также с терминальной стадией почечной недостаточности.
Таблица 5. Дозировка у пациентов детского возраста с нарушением функции почек, клиренс креатинина (КК) ≤ 50 мл/мин
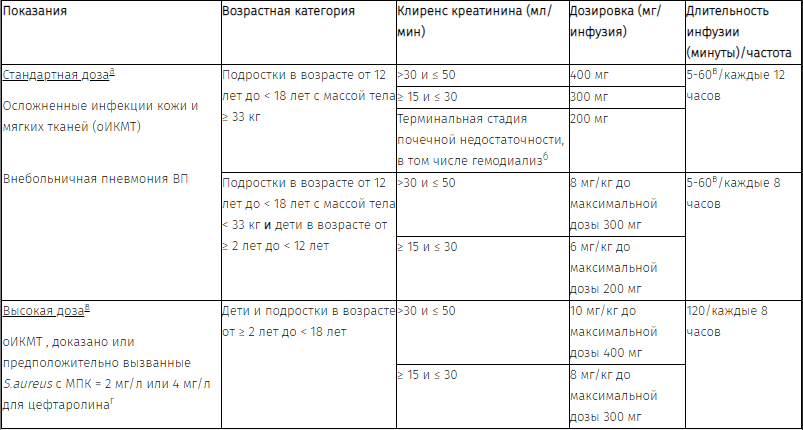
а Рассчитано по формуле Шварца для пациентов детского возраста (в мл/мин/1,73 м2). Доза основана на КК. КК следует тщательно контролировать, а дозу препарата следует корректировать в соответствии с функцией почек.
б Цефтаролин выводится при гемодиализе, поэтому препарат Зинфоро® необходимо вводить после выполнения гемодиализа в дни гемодиализа.
в Рекомендации по длительности инфузии менее 60 минут и применению высоких доз основаны только на результатах фармакокинетических и фармакодинамических анализов. См. разделы Особые указания, Фармакологические свойства.
г Для лечения инфекций, вызванных S.aureus, для которого МПК цефтаролина составляет ≤ 1 мг/л, рекомендуется стандартная доза препарата.
Нарушение функции печени
Нет необходимости корректировать дозу препарата у пациентов с нарушением функции печени.
Пожилые пациенты (≥65 лет)
Нет необходимости корректировать дозу препарата у пожилых пациентов с КК > 50 мл/мин.
Приготовление раствора для инфузий
При приготовлении и введении препарата необходимо соблюдать стандартные правила асептики. Каждый флакон предназначен только для однократного применения.
Препарат Зинфоро® порошок для приготовления концентрата для приготовления раствора для инфузий следует растворить в 20 мл стерильной воды для инъекций. Один мл концентрата содержит 30 мг цефтаролина фосамила. Полученный концентрат представляет собой раствор бледно-желтого цвета, свободный от видимых частиц. Концентрат необходимо немедленно использовать, не хранить (время от начала растворения порошка до полного приготовления раствора для внутривенных инфузий не должно превышать 30 минут).
Для приготовления раствора для инфузий полученный концентрат встряхивают и переносят в инфузионный флакон, содержащий одну из перечисленных ниже совместимых инфузионных жидкостей: 0,9% раствор натрия хлорида, 5% раствор декстрозы, 0,45% раствор натрия хлорида и 2,5% раствор декстрозы, раствор Рингер лактат.
При применении дозы препарата 600 мг во флакон с совместимой инфузионной жидкостью переносят весь полученный концентрат (20 мл), при применении дозы 400 мг 14 мл концентрата. Для применения дозы 300 мг следует перенести 10 мл концентрата, а для дозы 200 мг - 7 мл концентрата.
Раствор для инфузий можно приготовить путем добавления концентрата во флакон с инфузионной жидкостью объемом 50 мл, 100 мл или 250 мл.
Объем инфузионной жидкости у пациентов детского возраста зависит от массы тела. Концентрация раствора для инфузий в процессе его приготовления и введения не должна превышать 12 мг/мл цефтаролина фосамила.
После приготовления раствора для инфузий его следует использовать в течение 6 часов с момента приготовления. Приготовленный раствор для инфузий сохраняет стабильность в течение 24 часов при хранении в холодильнике (2-8оС). После извлечения из холодильника раствор для инфузий необходимо использовать в течение 6 часов при комнатной температуре.
Неиспользованный препарат или отходы необходимо утилизировать в соответствии с местными требованиями.
Препарат Зинфоро® показан к применению у новорожденных, младенцев, детей, подростков и взрослых для лечения следующих инфекций:
Препарат Зинфоро® может применяться при лечении взрослых пациентов с вторичной бактериемией, ассоциированной с осложненной инфекцией кожи и мягких тканей и внебольничной пневмонией. Недостаточно данных, позволяющих рекомендовать применение препарата Зинфоро® при лечении пациентов детского возраста с вторичной бактериемией, ассоциированной с осложненной инфекцией кожи и мягких тканей и внебольничной пневмонией.
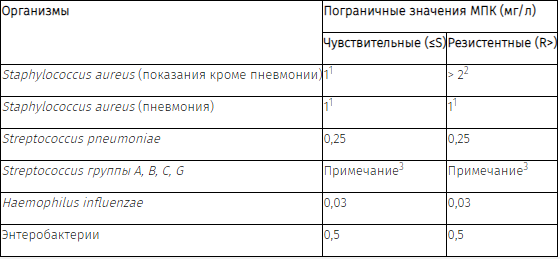
Чувствительность антибиотиков in vitro меняется в зависимости от географического региона и с течением времени, поэтому при выборе антибактериальной терапии необходимо учитывать местную информацию о резистентности.
При температуре не выше 30 °С. Хранить в местах, недоступных для детей.
Ограниченные данные по пациентам, получавшим препарат Зинфоро® в дозах, превышавших рекомендуемые, показывают нежелательные реакции, аналогичные наблюдавшимся у пациентов, получавших препарат в рекомендуемых дозах. Относительные передозировки могли возникать у пациентов с умеренным нарушением функции почек. При лечении передозировки необходимость следовать стандартной медицинской практике.
Цефтаролин можно удалить с помощью гемодиализа; в течение 4-часового периода диализа приблизительно 74 % полученной дозы выводилось с диализатом.
Не проводилось исследований по изучению влияния препарата Зинфоро® на способность к вождению автотранспорта и управлению иными механизмами. Во время терапии могут возникать нежелательные явления (например, головокружение), поэтому следует соблюдать осторожность при управлении транспортными средствами и при занятиях другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций. При появлении описанного выше нежелательного явления следует воздержаться от выполнения указанных видов деятельности.
В 1 флаконе содержится:
Действующее вещество: цефтаролина фосамила ацетат моногидрат 668,4 мг, эквивалентный цефтаролину фосамилу 600,0 мг;
Вспомогательное вещество: L-аргинин 395,0 мг.
Максимальная концентрация (Сmах) и площадь под кривой "концентрация-время" (AUC) цефтаролина увеличиваются почти пропорционально дозе при однократном введении препарата в диапазоне доз от 50 до 1000 мг.
Не наблюдалось заметной кумуляции цефтаролина после многократного внутривенного введения препарата в дозе 600 мг в течение 60 минут каждые 12 часов в течение 14 дней здоровым добровольцам с нормальной функцией почек.
Наблюдались аналогичные показатели системного воздействия (AUC), периода полувыведения цефтаролина (Т1/2) и клиренса цефтаролина после введения 600 мг цефтаролина фбсамила здоровым добровольцам в объеме 50 мл каждые 8 часов в течение 5дней в виде 5 минутной или 60 минутной инфузии, и время достижения максимальной концентрации (Тmах) цефтаролина составило 5 минут после окончания инфузии цефтаролина фосамила для обеих продолжительностей инфузии.
Среднее значение (SD) Сmах цефтаролина составило 32,5 (4,82) мг/л при продолжительности инфузии 5 минут (n=11) и 17,4 (3,87) мг/л при продолжительности инфузии 60 минут (n=12).
Распределение
Степень связывания цефтаролина с белками плазмы низкая (примерно 20%), препарат не проникает в эритроциты. Медиана объема распределения в равновесном состоянии у здоровых взрослых мужчин после однократного внутривенного введения 600 мг цефтаролина фосамила, меченного изотопом, составила 20,3 л, почти как и объем внеклеточной жидкости.
Метаболизм
В плазме крови под действием фосфатаз пролекарство цефтаролина фосамил быстро преобразуется в активный цефтаролин; концентрации пролекарства поддаются измерению в плазме, преимущественно, во время внутривенной инфузии.
При гидролизе бета-лактамного кольца цефтаролина образуется микробиологически неактивный метаболит, цефтаролин М-1. Соотношение средних значений AUC цефтаролина М-1 к цефтаролину в плазме крови после однократного внутривенного введения 600 мг цефтаролина фосамила здоровым добровольцам составляет примерно 20-30%.
Метаболизм цефтаролина протекает без участия изоферментов системы цитохрома Р450.
Экскреция
Цефтаролин выводится преимущественно почками. Почечный клиренс цефтаролина примерно равен или немного ниже скорости клубочковой фильтрации в почках. Исследования транспортеров in vitro показывают, что активная секреция не способствует почечной элиминации цефтаролина.
Средний период полувыведения цефтаролина у здоровых взрослых людей составляет примерно 2,5 часа. После однократного внутривенного введения 600 мг меченного изотопом цефтаролина фосамила здоровым взрослым мужчинам примерно 88% радиоактивности обнаруживалось в моче и 6% - в фекалиях.
Особые группы пациентов
Нарушение функции почек
После однократной внутривенной инфузии 600 мг цефтаролина фосамила в течение 60 минут Сmах цефтаролина в плазме составила 28,4 ± 6,9 мкг/мл, 28,2 ± 5,4 мкг/мл и 30,8 ± 4,9 мкг/мл у пациентов с нормальной функцией почек, нарушением функции почек легкой степени и нарушением функции почек средней степени тяжести, соответственно. Сmах цефтаролина достигалась приблизительно через 60 минут после начала инфузии.
AUC цефтаролина увеличивалась пропорционально степени нарушения функции почек и составила 75,6 ± 9,7 мкг.ч/мл, 92,3 ± 25,3 мкг.ч/мл и 114,8 ± 14,1 мкг.ч/мл у пациентов с нормальной функцией почек, нарушением функции почек легкой степени и нарушением функции почек средней степени тяжести, соответственно.
Коррекция дозы препарата требуется детям, подросткам и взрослым пациентам, если клиренс креатинина (КК) ≤ 50 мл/мин (см. раздел "Способ применения и дозы").
Недостаточно данных, позволяющих рекомендовать коррекцию дозы при терминальной стадии почечной недостаточности у подростков в возрасте от 12 до 18 лет с массой тела менее 33 кг и детей в возрасте от 2 до 12 лет.
Недостаточно данных, позволяющих рекомендовать коррекцию дозы у детей в возрасте до 2 лет с нарушением функции почек средней и тяжелой степени тяжести, а также с терминальной стадией почечной недостаточности.
Нарушение функции печени
Исследования фармакокинетики цефтаролина у пациентов с нарушением функции печени не проводили. Так как цефтаролин не подвергается печеночному метаболизму в значительной степени, не ожидается, что нарушение функции печени будет существенно влиять на системный Клиренс цефтаролина. Поэтому не рекомендуется корректировать дозу препарата у пациентов с нарушением функции печени.
Пожилые пациенты (≥ 65 лет)
После однократного внутривенного введения 600 мг цефтаролина фосамила параметры фармакокинетики препарата были схожими у здоровых пожилых людей (≥ 65 лет) и здоровых молодых пациентов (18-45 лет).
У пожилых добровольцев отмечено небольшое увеличение AUC0-∞ (на 33%), что обусловлено, главным образом, возрастными изменениями функции почек. Не требуется коррекции дозы препарата у пожилых пациентов с клиренсом креатинина выше 50 мл/мин.
Дети
Детям в возрасте от 2 месяцев до 12 лет и подросткам в возрасте от 12 до 18 лет с массой тела менее 33 кг требуется коррекция дозы (см. раздел "Способ применения и дозы"). Безопасность и эффективность препарата Зинфоро® у детей в возрасте до 2 месяцев не установлены.
Пол
Параметры фармакокинетики цефтаролина были схожими у мужчин и женщин. Не требуется коррекции дозы в зависимости от пола пациента.
Раса
Не наблюдалось существенных различий параметров фармакокинетики цефтаролина у пациентов, принадлежащих к разным этническим группам. Не требуется корректировать дозу препарата в зависимости от расы пациента.

Проверено фармацевтом
Фармацевт. Стаж – 43 года
Информация о товаре, включая его цену, носит ознакомительный характер и не является публичной офертой согласно ст 437 ГК РФ