
Проверено фармацевтом
Шемякина Лада Владимировна
В команде с марта 2023 годаФармацевт. Стаж – 5 лет
Избранные аптеки
0Москва и Московская область
Москва и Московская область
Клиентский сервис работает с 8.00 до 22.00
Клиентский сервис работает с 8.00 до 22.00
Есть противопоказания, проконсультируйтесь с врачом
Часто ищут в инструкции
Есть противопоказания, проконсультируйтесь с врачом
Цена: 4 434 ₽
Цена действительна при заказе на сайте
Товар добавлен
В корзинуДанный товар есть с меньшим сроком годности
Забронировать по сниженной цене можно по телефону
8 (495) 419 19 19Аналоги
Гипогликемическое средство для перорального применения комбинированное.
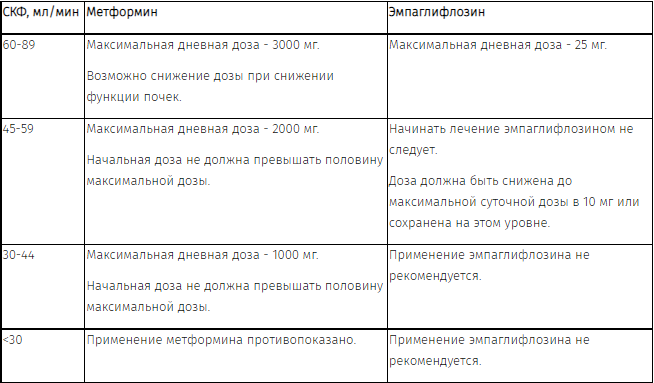
Метформин выводится почками, из-за возможного снижения функции почек необходимо корректировать дозу метформина под регулярным контролем показателей функции почек (определение концентрации креатинина в плазме крови не менее 2-4 раз в год).
Дети и подростки
Применение у детей и подростков до 18 лет противопоказано в связи с недостаточностью данных по эффективности и безопасности.
Пациенты с нарушением функции печени
Применение препарата СИНДЖАРДИ у пациентов с нарушением функции печени противопоказано.
Действия при пропуске приема одной или нескольких доз лекарственного препарата
При пропуске дозы, пациенту следует принять препарат, как только он об этом вспомнит. Не следует принимать двойную дозу в один день.
Повышенная чувствительность к эмпаглифлозину, метформину или любому из вспомогательных веществ препарата;
сахарный диабет 1 типа;
диабетический кетоацидоз;
диабетическая прекома, кома;
почечная недостаточность при СКФ < 45 мл/мин/1,73 м2;
острые состояния, протекающие с риском развития нарушения функции почек: дегидратация (при диарее или рвоте); тяжелые инфекционные заболевания, шок;
клинически выраженные проявления острых или хронических заболеваний, которые могут приводить к развитию тканевой гипоксии (в том числе, острая сердечная недостаточность, хроническая сердечная недостаточность с нестабильными показателями гемодинамики, дыхательная недостаточность, острый инфаркт миокарда);
печеночная недостаточность;
лактоацидоз;
острая алкогольная интоксикация, хронический алкоголизм;
беременность и период грудного вскармливания;
возраст 85 лет и старше;
детский возраст до 18 лет (в связи с недостаточностью данных по эффективности и безопасности);
применение в течение 48 часов до и в течение 48 часов после проведения радиоизотопных или рентгенологических исследований с введением йодсодержащего контрастного вещества;
соблюдение гипокалорийной диеты (менее 1000 ккал/сут);
обширные хирургические операции и травмы, когда показано проведение инсулинотерапии.
Заболевания желудочно-кишечного тракта, приводящие к потере жидкости;
диабетический кетоацидоз в анамнезе;
почечная недостаточность средней степени тяжести (СКФ 45-59 мл/мин/1,73 м2);
применение в комбинации с производными сульфонилмочевины или инсулином;
хроническая сердечная недостаточность со стабильными гемодинамическими показателями;
диета с очень низким содержанием углеводов;
злоупотребление алкоголем;
заболевания поджелудочной железы в анамнезе (панкреатит или операция на поджелудочной железе) или низкая секреторная активность бета-клеток поджелудочной железы;
при комбинированной терапии с инсулином - в случае снижения дозы инсулина;
совместное применение с гипотензивными препаратами, диуретиками и нестероидными противовоспалительными препаратами (НПВП);
при инфекциях мочевыводящих путей;
возраст старше 75 лет.
В клинических исследованиях наиболее часто сообщавшимся нежелательным явлением была гипогликемия, которая зависела от типа фоновой терапии, использовавшейся в соответствующих исследованиях, инфекции мочевыводящих и половых путей, увеличение мочеотделения.
В клинических исследованиях с применением эмпаглифлозина в комбинации с метформином каких-либо дополнительных нежелательных реакций по сравнению с нежелательными реакциями, отмечавшимися при использовании отдельных компонентов, не наблюдалось.
Нежелательные реакции распределены по системно-органным классам с указанием частоты их возникновения согласно рекомендациям ВОЗ: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000) или очень редко (<1/10000); выделяются также нежелательные реакции, частота которых неизвестна (не может быть оценена на основании имеющихся данных).
Нежелательные реакции, зарегистрированные в клинических исследованиях и в пострегистрационном периоде наблюдения:
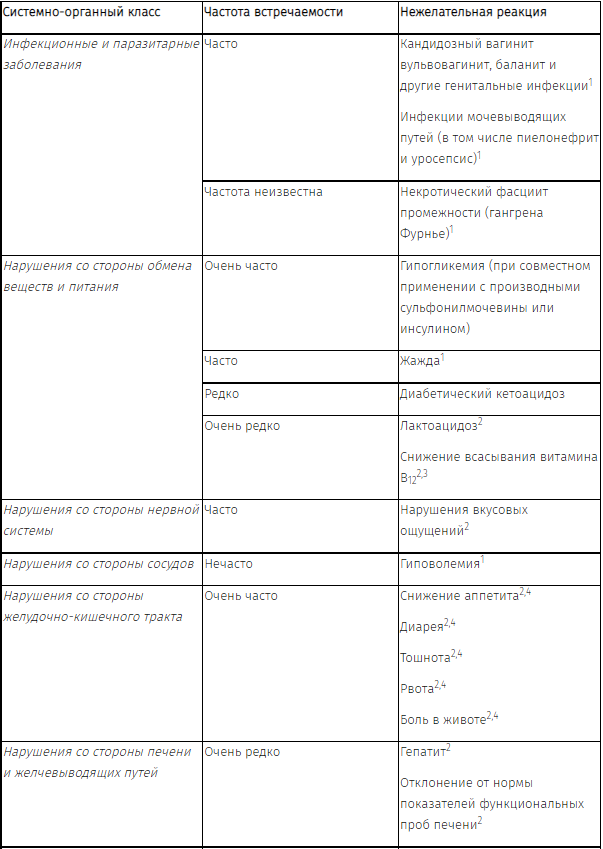
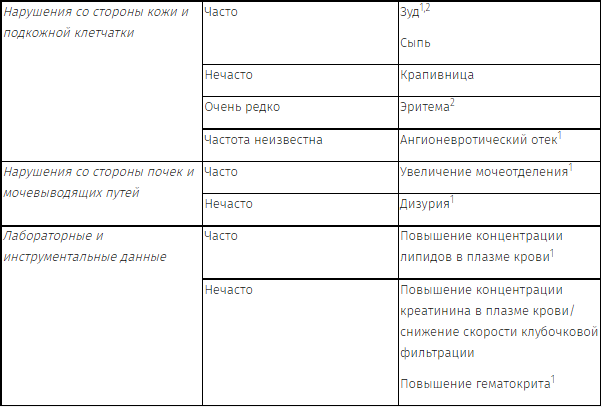
1 нежелательные реакции, зафиксированные при монотерапии эмпаглифлозином;
2 нежелательные реакции, зафиксированные при монотерапии метформином;
3 длительное лечение метформином сопровождалось снижением всасывания витамина В12, которое в очень редких случаях могло приводить к клинически значимому дефициту витамина B12, например, к мегалобластной анемии;
4 желудочно-кишечные симптомы, такие как снижение аппетита, диарея, тошнота, рвота и боль в животе наиболее часто появлялись в самом начале терапии и спонтанно исчезали в большинстве случаев.
Описание отдельных нежелательных реакций
Гипогликемия
Частота гипогликемии зависела от применявшейся сопутствующей гипогликемической терапии и была сравнима для эмпаглифлозина и плацебо при применении в комбинации с метформином, в комбинации с линаглиптином и метформином, для комбинации эмпаглифлозина с метформином у пациентов, ранее не получавших лечения в сравнении с пациентами, получавшими эмпаглифлозин и метформин как отдельные препараты и как дополнение к стандартной терапии. В случае назначения эмпаглифлозина в комбинации с производными сульфонилмочевины + метформин (эмпаглифлозин 10 мг: 16,1%, эмпаглифлозин 25 мг: 11,5%, плацебо: 8,4%) или в комбинации с инсулином + метформин (эмпаглифлозин 10 мг: 31,3%, эмпаглифлозин 25 мг: 36,2%, плацебо: 34,7%) частота развития гипогликемии была выше, чем в случае использования плацебо.
Тяжелая гипогликемия (требующая медицинского вмешательства)
Доля пациентов с тяжелой гипогликемией была невысокой (менее 1%) и сравнимой для эмпаглифлозина и плацебо при применении в комбинации с метформином, и для комбинации эмпаглифлозина с метформином у пациентов, ранее не получавших лечения, в сравнении с пациентами, получавшими эмпаглифлозин и метформин как отдельные препараты и как дополнение к стандартной терапии. Частота случаев тяжелой гипогликемии составляла 0,5%, 0% и 0,5% при применении эмпаглифлозина 10 мг, эмпаглифлозина 25 мг и плацебо, соответственно, на фоне терапии метформином в комбинации с инсулином. При применении эмпаглифлозина на фоне терапии метформином в комбинации с препаратами сульфонилмочевины, а также на фоне терапии метформином в комбинации с линаглиптином ни одного случая тяжелой гипогликемии не наблюдалось.
Инфекции мочевыводящих путей
Частота развития инфекций мочевыводящих путей в случае применения эмпаглифлозина в дозе 10 мг в комбинации с метформином была выше (8,8%), чем в случае применения эмпаглифлозина в дозе 25 мг в комбинации с метформином (6,6%) или плацебо в комбинации с метформином (7,8%). Так же, как и в случае применения плацебо, инфекции мочевыводящих путей чаще отмечались у пациентов с хроническими и рецидивирующими инфекциями мочевыводящих путей в анамнезе. Тяжесть инфекций мочевыводящих путей была сходной у пациентов, принимающих эмпаглифлозин и плацебо.
Об инфекциях мочевыводящих путей чаще сообщалось у женщин, получавших эмпаглифлозин в дозе 10 мг в комбинации с метформином, чем у женщин, получавших плацебо; этого не наблюдалось в случае применения эмпаглифлозина в дозе 25 мг в комбинации с метформином. Частота инфекций мочевыводящих путей у мужчин была небольшой и схожей в лечебных группах.
Генитальные инфекции
Частота развития таких нежелательных явлений как кандидозный вагинит, вульвовагинит, баланит и других генитальных инфекций была выше в случае применения эмпаглифлозина в дозе 10 мг в комбинации с метформином (4,0%) и эмпаглифлозина в дозе 25 мг в комбинации с метформином (3,9%), чем при применении плацебо или плацебо в комбинации с метформином (1,3%). Эти различия в частоте были менее заметными у мужчин. Нежелательные реакции со стороны половых органов были легкой и средней степени тяжести.
Увеличение мочеотделения
Частота случаев увеличенного мочеотделения (оценивались такие симптомы, как поллакиурия, полиурия, никтурия) была выше в случае применения эмпаглифлозина в дозе 10 мг в комбинации с метформином (3,0%) и эмпаглифлозина в дозе 25 мг в комбинации с метформином (2,9%), чем в случае применения плацебо в комбинации с метформином (1,4%). Частота развития никтурии была сопоставима в группе пациентов, принимавших эмпаглифлозин в комбинации с метформином и в группе пациентов, принимавших плацебо в комбинации с метформином (менее 1%). Интенсивность увеличенного мочеотделения была легкой или умеренной.
Гиповолемия
Частота развития гиповолемии (которая выражалась снижением артериального давления, ортостатической артериальной гипотензией, дегидратацией, обмороком) при применении эмпаглифлозина в комбинации с метформином была низкой или сопоставимой с плацебо (эмпаглифлозин в дозе 10 мг в комбинации с метформином (0,6%), эмпаглифлозин в дозе 25 мг в комбинации с метформином (0,3%), плацебо в комбинации с метформином (0,1%). Глюкозурический эффект эмпаглифлозина сопровождается осмотическим диурезом, который может оказывать влияние на состояние гидратации пациентов в возрасте 75 лет и более. У пациентов в возрасте ≥ 75 лет сообщалось об одном случае гиповолемии у пациента, получающего эмпаглифлозин в дозе 25 мг в качестве дополнения к терапии метформином.
Снижение скорости клубочковой фильтрации и повышение концентрации креатинина в крови
Общая частота снижения скорости клубочковой фильтрации и повышения концентрации креатинина в крови были схожи при применении эмпаглифлозина и плацебо с метформином (повышение концентрации креатинина в крови: эмпаглифлозин 10 мг 0,5%, эмпаглифлозин 25 мг 0,1%, плацебо 0,4%; Снижение скорости клубочковой фильтрации: эмпаглифлозин 10 мг 0,1%, эмпаглифлозин 25 мг 0%, плацебо 0,2%). Наблюдалось начальное транзиторное повышение концентрации креатинина в крови (среднее изменение по сравнению с исходным значением после 12 недель: эмпаглифлозин в дозе 10мг- 0,02 мг/дл, эмпаглифлозин в дозе 25 мг - 0,02 мг/дл) и начальное транзиторное снижение расчетной скорости клубочковой фильтрации (среднее изменение по сравнению с исходным значением после 12 недель: эмпаглифлозин в дозе 10 мг - 1,46 мл/мин/1,73 м2, эмпаглифлозин в дозе 25 мг - 2,05 мл/мин/1,73 м2). В долгосрочных исследованиях эти изменения обычно были обратимыми при продолжении лечения или после прекращения приема препарата.
Препарат СИНДЖАРДИ показан для терапии сахарного диабета 2 типа у взрослых пациентов в качестве дополнения к диетотерапии и физическим упражнениям с целью улучшения гликемического контроля:
при неудовлетворительном гликемическом контроле на фоне монотерапии метформином в максимально переносимой дозе;
в комбинации с другими гипогликемическими препаратами при неудовлетворительном гликемическом контроле на фоне их совместного применения с метформином;
у пациентов, которые ранее получали комбинированную терапию эмпаглифлозином и метформином в виде отдельных препаратов.
Хранить при температуре не выше 25 °С. Хранить в недоступном для детей месте.
Симптомы
Во время проведения контролируемых клинических исследований при однократном приеме эмпаглифлозина в дозе 800 мг (в 32 раза превышавшей максимальную суточную дозу) здоровыми добровольцами препарат переносился хорошо.
При применении метформина в дозах, достигавших 85 г, гипогликемия не наблюдалась, однако в ряде случаев это привело к развитию лактоацидоза. Значительная передозировка метформином или наличие сопутствующих факторов риска может привести к лактоацидозу.
Лактоацидоз относится к категории неотложных медицинских ситуаций, лечение в таких случаях должно проводиться в стационаре.
Лечение
В случае передозировки рекомендуется удаление неабсорбированного препарата из желудочно-кишечного тракта, осуществление клинического контроля и проведение симптоматического лечения.
Самым эффективным методом выведения лактата и метформина является гемодиализ; возможность выведения эмпаглифлозина с помощью гемодиализа не изучалась.
Исследований по влиянию препарата СИНДЖАРДИ на способность управлять транспортными средствами и механизмами не проводилось. Однако в связи с возможным развитием гипогликемии (которая может проявляться в виде головной боли, сонливости, слабости, головокружения, спутанности сознания, раздражительности, голода, учащенного сердцебиения, потливости, панических атак), особенно при приеме препарата СИНДЖАРДИ в комбинации с производными сульфонилмочевины и/или инсулином, необходимо соблюдать осторожность при управлении транспортными средствами и механизмами.
Действующие вещества: метформина гидрохлорид - 1000,000 мг; эмпаглифлозин - 5,000 мг;
вспомогательные вещества: крахмал кукурузный - 65,260 мг, коповидон - 94,400 мг, кремния диоксид коллоидный безводный - 5,900 мг, магния стеарат - 9,440 мг;
пленочная оболочка: Опадрай® желтый (02В220012) - 19,00 мг (гипромеллоза 2910 - 9,500 мг, макрогол 400 - 0,950 мг, титана диоксид - 2,156 мг, краситель железа оксид желтый - 2,594 мг. тальк - 3,800 мг).

Проверено фармацевтом
Фармацевт. Стаж – 5 лет
Информация о товаре, включая его цену, носит ознакомительный характер и не является публичной офертой согласно ст 437 ГК РФ